آمبولی ریه
آمبولی ریه (Pulmonary Embolism)
ارائه دهندگان: Jessica Mason MD, Mel Herbert MD, Stuart Swadron MD
بازبین علمی: Anand Swaminathan, MD
*دوز داروها صرفا به عنوان راهنما ذکر شدهاند. همیشه از منبع دیگری نیز استفاده کنید و از پروتکلهای محلی پیروی کنید.
نکات کلیدی
- در تشخیص آمبولی ریه (PE)اولین گام ارزیابی احتمال اولیه (Pre-test Probability) است.
- پزشکان باتجربه میتوانند از قضاوت بالینی (Clinical Gestalt) استفاده کنند.
- ابزارهای تصمیمگیری مانند امتیازبندی ولز (Wells score) یا ژنو (Geneva score) نیز کاربرد دارند.
- احتمال PE در بیماران کمخطر با ریسک پایین (احتمال آمبولی ریه کمتر از 2%) را میتوان با استفاده از PERC rule یا D-dimer منفی رد کرد.
- قانون PERC میتواند نیاز به تستهای بیشتر را حذف کند.
- از مقادیر تعدیلشده D-dimer میتوان در بیماران بالای 50 سال استفاده کرد
- فرمول FEUs(Fibrinogen Equivalent Units) : سن × 10
- DDUs(D Dimer Units): سن × 5
- بیماران با ریسک متوسط بحثبرانگیزتر هستند.
- برخی پروتکلها استفاده از D-dimer را توصیه میکنند، در حالی که برخی دیگر منابع مستقیماً مسیر تصویربرداری را پیش میگیرند.
- در بیماران پرخطر باید مستقیماً مسیر تصویربرداری را پیش بگیریم
- گزینههای تصویربرداری شامل سیتی آنژیوگرافی ریوی(CT pulmonary angiography – که در اغلب پروتکلها استفاده میشود)، اسکن تهویه-پرفیوژن (V/Q-ventilation-perfusion scanning) و سونوگرافی دوطرفه اندامهای تحتانی است.
- در بیماران پرخطر بدون کنترااندیکاسیون، شروع داروی آنتیکوآگولاون قبل از آمدن نتایج تستهای قطعی اقدام مناسبی است.
- درمان اولیه شامل هپارین تجزیه نشده(unfractionated heparin) ، هپارین با وزن مولکولی پایین(low molecular weight heparin) یا آنتیکوآگولان مستقیم خوراکی(direct oral anticoagulant) است.
- ترومبولیتیکها (مانند آلتپلاز) برای بیماران دچار شوک (مثلا افت فشار خون) نگه داشته میشوند.
- مدیریت بیماران باردار مشکوک به PE باید بر اساس سیاستها، منبع و پروتکلهای محلی انجام شود.
پیشزمینه:
ترومبوآمبولی وریدی (Venous thromboembolism – VTE)لختههای غیرطبیعی در وریدها میتوانند در سراسر بدن ایجاد شوند. شایعترین نوع آن ترومبوز ورید عمقی (deep venous thrombosis – DVT) در پاها است، اما ممکن است در اندام فوقانی، لگن و حتی سینوسهای وریدی مغز نیز رخ دهد. علاوه بر این، ترومبوز ورید عمقی (DVT) و آمبولی ریه (PE) در یک طیف گسترده قرار دارند که میتواند از موارد خفیف یا حتی بدون علائم بالینی تا شرایط تهدیدکننده حیات متغیر باشد و منجر به هیپوکسی شدید و اختلال شدید همودینامیک شود.
آمبولی ریه زمانی رخ میدهد که یک لخته (آمبولی) از طریق سیستم گردش وریدی و قلب راست به شریانهای ریوی منتقل شود. بنابراین، DVT و PE مراحل مختلفی از یک فرآیند پاتولوژیک مشابه را توصیف میکنند. درواقع PE در 40% از بیماران مبتلا به DVT یافت میشود. به طور متقابل نیز در 70% از بیماران مبتلا به PE، DVT تشخیص داده میشود.
در این اپیزود، ما بر روی بیماران مبتلا به PE تمرکز میکنیم و پس از بحث در مورد ویژگیهای کلیدی در شرح حال، معاینه و ECGبه بررسی ابزارهای ارزیابی ریسک(risk stratification tools)، روشهای تشخیصی و مدیریت بیماران پایدار، بیماران بحرانی و جمعیتهای خاص (مانند بیماران باردار) میپردازیم.
ارزیابی بالینی
- پاتوفیزیولوژی در آمبولی ریه: چرا این بیماری اینقدر خطرناک است؟
- ناسازگاری تهویه/پرفیوژن (Ventilation/perfusion (V/Q) mismatch)
- پارانشیم ریه تهویه میشود اما خون یا اکسیژن دریافت نمیکند.
- افزایش فشار شریان ریوی–> نارسایی قلب راست –> نهایتا پرفیوژن ضعیف شریان کرونری.
- ناسازگاری تهویه/پرفیوژن (Ventilation/perfusion (V/Q) mismatch)
- شرح حال کلاسیک
- علائم DVT
- اندام دردناک، متورم و قرمز
- علائم PE
- تنگی نفس؛ تقریباً ۸۰٪ از بیماران با PE حاد دچار تنگی نفس هستند.
- درد قفسه سینه: تقریباً ۴۹٪ از بیماران با PE حاد دچار درد قفسه سینه هستند.
- شکایت کلاسیک، درد pleuritic (درد هنگام دم) است.
- هموپتیزی
- ممکن است رخ دهد اما نادر است.
- به یاد داشته باشید شایعترین علت هموپتیزی برونشیت(bronchitis) است.
- سنکوپ
- عوامل خطر
- سابقه VTE، جراحی اخیر، بیحرکتی، بدخیمی، استفاده از قرصهای ضدبارداری خوراکی (OCP)/ مکمل تستوسترون، ترومبوفیلیا.
- معاینه فیزیکی
- یافتههای معاینه در DVT
- اندام قرمز، متورم و حساس در لمس(tender) به صورت یکطرفه.
- ممکن است بهاشتباه شبیه سلولیت به نظر برسد.
- علامت هومن(Homan’s sign)
- دورسی فلکشن پا باعث درد در پشت ساق(calf tenderness) پا میشود.
- این علامت بهصورت کلاسیک در دانشگاه آموزش داده میشود شده اما حساسیت یا ویژگی کافی ندارد.
- طناب قابل لمس(Palpable cord)
- ساختار وریدی تندر، سفتشده(indurated) و شبیه طناب(cordlike)
- این علامت ترومبوفلبیت سطحی است که میتواند با DVT همراهی داشته باشد.
- وجود گچ روی اندام مبتلا(نشان بیحرکتی و عامل خطری برای DVT)
- اندام قرمز، متورم و حساس در لمس(tender) به صورت یکطرفه.
- یافتههای معاینه در PE
- تاکیپنه
- تاکیکاردی؛ تنها ۲۴-۳۰٪ از بیماران تاکیکاردی دارند.
- هیپوکسی
- کراکلها
- تب، سیانوز (کمتر شایع)
- یافتههای معاینه در DVT
- علائم DVT
- ECG
- یافتههای کلاسیک (نگاه کنید به جدول ۱):
- همچنین در EMRAP اکتبر ۲۰۱۶ توسط Jeff Kline به این مطلب پرداخته شده است:
Table 1. ECG Findings in Pulmonary Embolism
| Nonspecific ECG changes Sinus tachycardia Right axis deviation Right bundle branch block S1Q3T3 (uncommon) T wave inversion in the anterior leads (Wellens pattern) ST elevation in aVR Atrial fibrillation |
خلاصهی نکات اپیزود یافتههای کلاسیک ECG در PE:
- در صورتی که در ECG تظاهر T wave inversion in the anterior leads (Wellens pattern) را ببینیم احتمالا با PE وسیعی مواجه هستیم. همچنین این یافته در SAH نیز ممکن است دیده شود.
- وجود ST elevation in aVR پروگنوز را ضعیف میکند.
- الگوی S1Q3T3 که در دانشگاه نیز اغلب زیاد بر آن تاکید میشود غیر حساس و غیر اختصاصی است.
- تاکیکاردی نیز تنها در 30-24% افراد مبتلا به PE دیده میشود.
طبقهبندی خطر(RISK STRATIFICATION) و تشخیص
- اهداف طبقهبندی خطر
- تصمیمگیری در مورد اینکه چه کسانی نیاز به آزمایش دارند یا ندارند.
- تعیین اینکه چه نوع آزمایش و تصویربرداری مناسب است.
- تصمیمگیری در مورد اینکه چه کسانی به درمان تجربی نیاز دارند.
- جلوگیری از قرار گرفتن بیماران با ریسک پایین در معرض اشعه!
- ظن بالینی (Clinical Gestalt)
- عملکردی مشابه امتیازهای Wells و Revised Geneva دارد.
- هشدار: برای داشتن Clinical Gestalt، نیاز به تجربه بالینی دارید.
- کرایتریای (Pulmonary Embolism Rule-out Criteria)PERC – (جدول 2 را نگاه کنید)
- برای تعیین اینکه آیا اصلاً نیازی به آزمایش و تصویربرداری وجود دارد یا خیر.
- برای اعمال این قانون باید pretest probability ما کم باشد(کمتر از 15) وگرنه نمیتوانیم از آن استفاده کنیم(مترجم:درواقع ابتدا با استفاده از امتیازبندی Wells یا Geneva یا اگر تجربه داریم با استفاده از گشتالت بالینی خود یک درصدی از احتمال PE در ذهنمان متصور میشویم و اگر این تخمین کمتر از 15% بود میتوانیم از معیارهای PERC استفاده کنیم)
- اگر هیچکدام از معیارهای PERC وجود نداشته باشند و pretest probability کمتر از 15%باشد، نیازی به آزمایش بیشتر نیست.
- اگر هر یک از معیارهای PERC وجود داشته باشد:
- برخی پزشکان D-dimer را درخواست میکنند یا قانون PERC را با امتیاز Wells دنبال میکنند.
- به یاد داشته باشید PERC همه چیز را شامل نمیشود و هیچ قانون و معیار تصمیمگیری نمیتواند جایگزین ظن بالینی(gestalt) شما شود.
- Wells Score (به جدول3 نگاه کنید)
- گروههای کمخطر، خطر متوسط و پرخطر بر اساس امتیاز تعیین میشوند
- کمخطر(امتیاز کمتر از2)
- برخی پزشکان از معیار PERC استفاده میکنند، در حالی که برخی دیگر D- dimer درخواست میکنند.
- خطر متوسط (6-2 امتیاز)
- برخی پزشکان D-dimer درخواست میکنند، در حالی که برخی دیگر آنژیوگرافی ریوی با سیتی (CT Pulmonary Angiography) انجام میدهند.
- پرخطر(امتیاز بیشتر از 6)
- آنژیوگرافی ریوی با سیتی(CT Pulmonary Angiography)
- خطر متوسط (6-2 امتیاز)
- برخی پزشکان از معیار PERC استفاده میکنند، در حالی که برخی دیگر D- dimer درخواست میکنند.
- Revised Geneva Score
- با وجود ابزارهای متعدد طبقهبندی خطر، این امتیاز دیگر به اندازه گذشته استفاده نمیشود، اما همچنان یک گزینه است.
- رویکرد یک متخصص(expert)
- کمخطر(خطر کمتر از 20% ) : استفاده ازPE Rule Out Criteria (PERC) یا D-dimer
- خطر متوسط (20-40%): CT Pulmonary Angiography
- پرخطر(خطر بیشتر از 40%): شروع هپارین تجربی، CT Pulmonary Angiography و ممکن است به آزمایشهای اضافی برای رد ترومبوز ورید عمقی (مانند سونوگرافی اندامها) نیاز باشد.
- D-dimer متناسب شده با سن(Age adjusted D-dimer)
- حد بالای نرمال برای بیماران بالای 50 سال:
- سن 10xبرای آزمایش و Fibrinogen Equivalent Units (FEUs)
- سن 5x برای آزمایش D Dimer Units (DDUs)
- به نظر میرسد که این روش، ویژگی را افزایش میدهد بدون اینکه حساسیت را تحت تأثیر قرار دهد.
- حد بالای نرمال برای بیماران بالای 50 سال:
- CT pulmonary angiography (CTPA)
- به دنبال نقصهای پرشدگی(filling defects)، علائم نارسایی قلب راست یا انفارکتوس ریوی میگردد.
- همچنین در CTPA به دنبال علل دیگری که میتواند منجر به این علائم شود میگردیم.
- اسکن تهویه-پرفیوژن(Ventilation perfusion (V/Q) scan)
- مرور
- تهویه(Ventilation) – بیمار یک گاز بیضرر با ایزوتوپ رادیواکتیو (مانند زنون-133، کریپتون-81) را تنفس میکند.
- پرفیوژن: تکنسیوم-99 تزریق میشود و پرفیوژن ارزیابی میگردد.
- ابتدا باید یک عکس قفسه سینه(CXR) طبیعی برای ارزیابی هرگونه نقص تهویهای]مثلا پنومونی یا توده[ داشته باشید، سپس میتوانید اسکن V/Q را انجام دهید.
- به دنبال عدم تطابقی(mismatch) بگردید که در آن بخشی از ریه تهویه میشود اما پرفیوژن ندارد، که نشاندهنده وجود لخته خون است.
- نتایج به دستههای نرمال، احتمال پایین، احتمال متوسط و احتمال بالا تقسیم میشوند.
- مرور
Table 2. PERC Criteria*
| PERC Criteria* |
| Age ≥50 |
| Heart rate ≥100 at triage |
| Oxygen saturation <95% |
| Unilateral leg swelling |
| Hemoptysis |
| Recent surgery or trauma ≤4 weeks, requiring general anesthesia |
| Prior PE or DVT |
| Hormone use Oral contraceptives, hormone replacement therapy, or estrogen use |
اگر هیچیک از معیارهای PERC وجود نداشته باشد و pretest probability پزشک کمتر از ۱۵٪ باشد، نیازی به انجام آزمایشهای بیشتر نیست.
اقتباس شده از کلاین، 2008
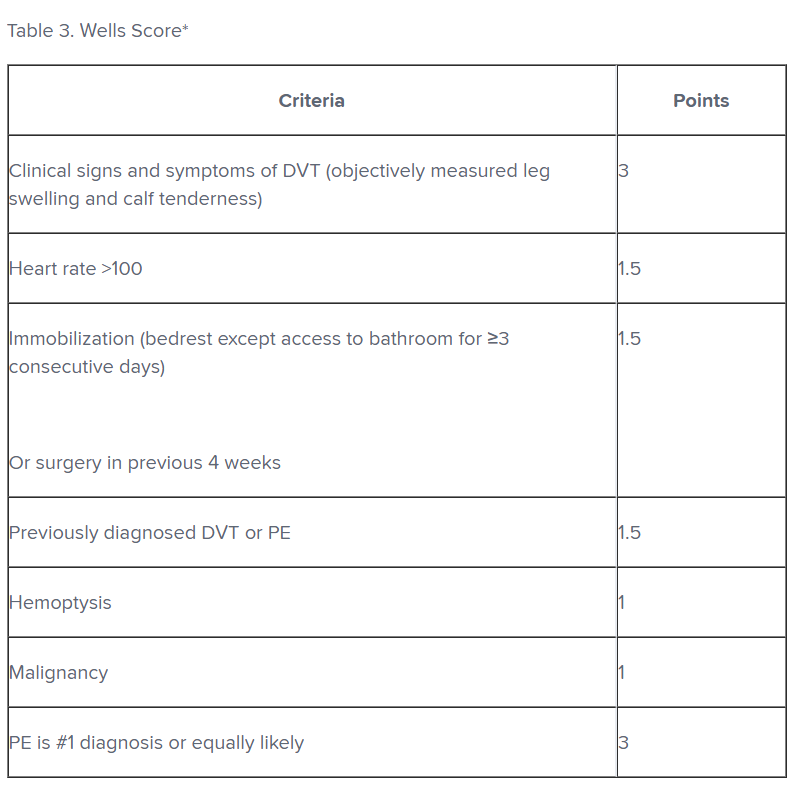
Score <2 = low risk (1.3% prevalence)
Score 2-6 = moderate risk
Score >6 = high risk
اقتباس شده از ولز، 2001
پیشبرد تشخیصی آمبولی ریه در بیماران باردار
- بارداری
- یک افسانهی رایج وجود دارد که بیماران باردار خطر بسیار بیشتری برای PE نسبت به بیماران غیر باردار دارند. این باور موجب انجام آزمایشهای بیش از حد در بیماران باردار شده است
- بیشتر این مطالعات اپیدمیولوژیک، DVT را با PE و بارداری را با بیماران پس از زایمان(postpartum) ترکیب کردهاند]مثلا اختصاصا روی PE کار نکردهاند یا اختصاصا روی زنان باردار مطالعه نکردهاند و پست پارتوم را نیز شامل مطالعه کردهاند).
- در واقع ثابت شده است که تنها افزایش بسیار کمی در بروز این خطر وجود دارد
- آمبولی ریه در حدود 3 نفر از 10,000 بارداری رخ میدهد (میانگین در طول دوره بارداری)
- در اینها خطر بیشتر است
- همراه با DVT
- در هر سه ماهه بارداری
- بعد از زایمان
- با زایمان سزارین نسبت به زایمان واژینال
- یک افسانهی رایج وجود دارد که بیماران باردار خطر بسیار بیشتری برای PE نسبت به بیماران غیر باردار دارند. این باور موجب انجام آزمایشهای بیش از حد در بیماران باردار شده است
درمان آمبولی ریه در بیماران پایدار
- داروهای ضد انعقاد(Anticoagulation)
- داروهای ضد انعقاد خوراکی مستقیم (DOACs – Direct oral anticoagulation)
- گزینهها شامل موارد زیر است:
- ریواروکسابان (Rivaroxaban) یا اپیکسابان (Apixaban)
- میتوان این داروها را بلافاصله به صورت خوراکی شروع کرد و نیازی به ضد انعقاد تزریقی قبل از آن نیست.
- دابیگاتران (Dabigatran) و ادوکسابان (Edoxaban)
- مانند وارفارین، این داروها نیاز به ضد انعقاد تزریقی به مدت 5 تا 10 روز قبل از شروع دارند.
- انتخاب DOAC به هزینه/بیمه و بیماریهای همراه بستگی دارد:
- برخی از این داروها در صورت وجود بیماری کبدی منع مصرف دارند.
- این داروها برای بیمارانی که دیالیز میشوند، باردار هستند یا در دوران شیردهی قرار دارند، گزینه مناسبی نیستند.
- ریواروکسابان (Rivaroxaban) یا اپیکسابان (Apixaban)
- گزینهها شامل موارد زیر است:
- هپارین با وزن مولکولی پایین (Low molecular weight heparin [fractionated])
- انوکساپارین (Enoxaparin) (و دیگر داروها) – تزریق زیرجلدی
- 1میلیگرم/کیلوگرم هر 12 ساعت (در دوران بارداری)، یا
- 1.5میلیگرم/کیلوگرم هر 24 ساعت (در غیر بارداری)
- هپارین درمانی پلزننده به وارفارین با هدف INR بین 2 تا 3 خواهد بود
- انوکساپارین (Enoxaparin) (و دیگر داروها) – تزریق زیرجلدی
- داروهای ضد انعقاد خوراکی مستقیم (DOACs – Direct oral anticoagulation)
- برنامه درمانی بلندمدت
- ممکن است به ضد انعقاد به مدت 3 ماه یا 6-12 ماه نیاز باشد.
- عوامل خطر(risk factors) گذرا: معمولاً نیاز به 3 ماه درمان دارد.
- عوامل خطر پایدار یا Venous thromboembolism بدون علت مشخص(unprovoked VTE) معمولاً نیاز به 12-6 ماه درمان دارد.
- عوامل خطر پایدار و خطر بالای عود ممکن است نیاز به ضد انعقاد مادامالعمر داشته باشد.
- ممکن است به ضد انعقاد به مدت 3 ماه یا 6-12 ماه نیاز باشد.
- تعیین وضعیت بیمار(Disposotion)
- میتوان مدیریت سرپایی را در نظر گرفت اگر بیمار ظاهر خوبی داشته باشد، پیگیری مناسب داشته باشد و توانایی تهیهی نسخه داروهای ضدانعقاد را داشته باشد.
- شاخص شدت آمبولی ریوی (PE severity index –PESI) و HESTIA criteria
- برای تصمیمگیری در مورد سطح مراقبت (اینکه چه کسی نیاز به بستری دارد و چه کسی میتواند با خیال راحت ترخیص شود) استفاده میشود.
- معیارهای PESI اصلی و سادهشده هر دو عملکرد خوبی دارند.
- نسخه اصلی PESI تعداد بیشتری از بیماران را بهعنوان کمخطر طبقهبندی میکند نسبت به نسخه سادهشده
- یک معیار را انتخاب کرده و امتیاز آن را محاسبه کنید؛ بسیاری از عوامل خطر بین این دو معیار همپوشانی دارند.
- بسیاری از عوامل خطر کاملاً واضح به نظر میرسند (مانند ناپایداری همودینامیک، سن بالا، سابقه سرطان، بیماری قلبی-ریوی، بارداری، بیماری کبد، شکست درمان سرپایی با ضد انعقاد، خونریزی فعال، سابقه ترومبوسیتوپنی ناشی از هپارین، وضعیت هوشیاری تغییر یافته).
- بیمار ایدهآل برای ترخیص: بیماری که از نظر بالینی ظاهر خوبی دارد، از نظر جسمی سالم است، آمبولی ریوی کوچک دارد، هیچ عامل خطر نگرانکنندهای ندارد، و از نظر مالی و اجتماعی قادر به تهیه داروها و مصرف منظم آنها است.
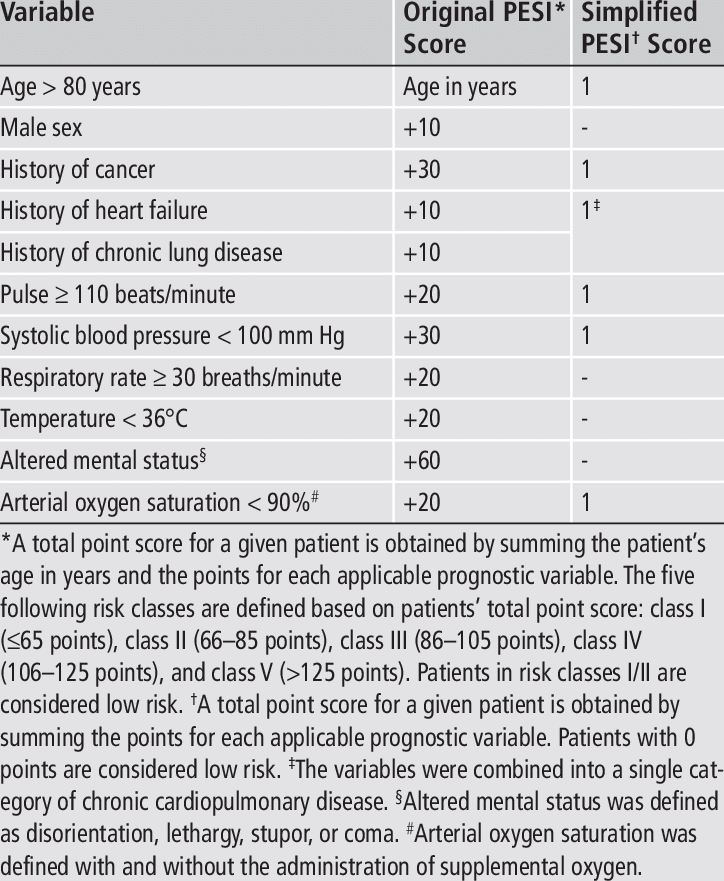
منبع: https://www.researchgate.net/figure/Original-and-simplified-Pulmonary-Embolism-Severity-Index-PESI_tbl1_51452185
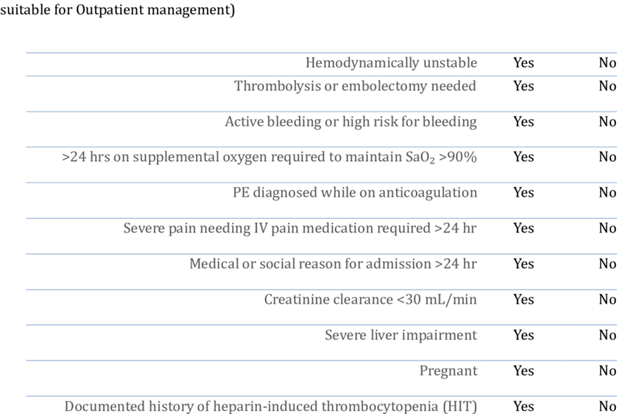
Hestia Criteria؛ اگر پاسخ به هر یک از معیارهای فوق “بله” باشد، بیمار واجد شرایط جهت درمان سرپایی تلقی نمیشود و باید بستری گردد.
ارزیابی و درمان بیمار بحرانی(critical)
- یافتههای سونوگرافی مطابق با تحت فشار قرار گرفتن قلب راست(right heart strain)
- به دلیل وجود لخته، فشار بالایی در شریانهای ریوی ایجاد شده که این فشار به بطن راست پس میزند(برگشت داده میشود) و منجر به موارد زیر میگردد:
- گشاد شدن بطن راست (RV dilation)
- در نمای سابزیفوئید، نسبت طبیعی RV به LV برابر با ⅓ به ⅔ است. هر نسبتی بزرگتر از این (مانند (RV >⅓ غیرطبیعی محسوب میشود.
- خمیدگی(Bowing) سپتوم به سمت بطن چپ(این حالت باعث ایجاد بطن چپ شکل “D” میشود )
- نمای Severe D Sign در اولتراسوند: https://www.emrap.org/episode/severedsign/severedsign
- علامت مککانل (McConnell’s sign)
- آکنزی (Akinesia – عدم حرکت) دیواره آزاد بطن راست با حرکت طبیعی در ناحیه آپکس.
- McConnell’s sign در اولتراسوند: https://www.emrap.org/episode/mcconnellssign/mcconnellssign
- گشاد شدن بطن راست (RV dilation)
- به دلیل وجود لخته، فشار بالایی در شریانهای ریوی ایجاد شده که این فشار به بطن راست پس میزند(برگشت داده میشود) و منجر به موارد زیر میگردد:
- درمان
- احیای با مایعات (Fluid resuscitation)
- احتیاط کنید! تزریق بیش از حد مایعات میتواند نارسایی قلب راست را تشدید کرده و باعث افزایش خمیدگی سپتوم به سمت بطن چپ شود.
- حمایت با وازوپرسورها (Pressor support)
- از وازوپرسورهایی مانند اپینفرین یا نوراپینفرین برای جلوگیری از افت فشار خون و پلزدن به درمان قطعیتر استفاده کنید.
- ضد انعقاد (Anticoagulation)
- اگر تجویز ترومبولیز (Thrombolysis) امکانپذیر باشد، استفاده از هپارین تجزیه نشده (Unfractionated Heparin) را در نظر بگیرید (نیمهعمر آن فقط ۱-۲ ساعت است).
- دوز شروع: ۸۰ واحد/کیلوگرم به صورت بولوس وریدی(80 U/kg IV bolus )، سپس انفوزیون مداوم با دوز ۱۶-۱۸ واحد/کیلوگرم در ساعت(16-18 U/kg/hr infusion)
- تنظیم دوز بر اساس مهار فاکتور Xa
- اگر تجویز ترومبولیز امکانپذیر نیست، از هپارین تجزیه شده (Fractionated Heparin) استفاده کنید:
- انوکساپارین: ۱ میلیگرم/کیلوگرم به صورت زیرجلدی
- اگر ضد انعقاد(anticoagulation) ممنوعیت مطلق دارد، استفاده از فیلتر IVC را در نظر بگیرید و زمانی که ایمن است، ضد انعقاد را شروع کنید.
- ممنوعیت مطلق ضد انعقاد:
- با رادیولوژیست مداخلهای(interventional radiologist) یا متخصص قلب درباره امکان آسپیراسیون لخته صحبت کنید.
- اگر تجویز ترومبولیز (Thrombolysis) امکانپذیر باشد، استفاده از هپارین تجزیه نشده (Unfractionated Heparin) را در نظر بگیرید (نیمهعمر آن فقط ۱-۲ ساعت است).
- ترومبولیز (Thrombolysis)
- درمان انتخابی برای آمبولی ریه گسترده – (Massive PE)به صورت افت فشار خون مداوم به مدت بیش از ۱۵ دقیقه به دلیل بار زیاد لخته تعریف میشود)
- بررسی موارد منع مطلق و نسبی (جدول ۴).
- آلتپلاز (Alteplase)– (مورد تأیید FDA برای PE)
- وزن بیشتر از ۶۵ کیلوگرم: ۱۰۰ میلیگرم وریدی (۱۰ میلیگرم به صورت بولوس وریدی، سپس ۹۰ میلیگرم در مدت ۲ ساعت).
- وزن کمتر از ۶۵ کیلوگرم: تنظیم دوز برای حفظ مقدار کمتر از ۱.۵ میلیگرم/کیلوگرم.
- این درمان علاوه بر شروع ضد انعقاد با هپارین انجام میشود.
- ترومبکتومی باز (Open Thrombectomy)
- برای بیمارانی که منع مصرف مطلق برای ترومبولیز سیستمیک دارند یا بهعنوان نجات پس از شکست ترومبولیز سیستمیک در نظر گرفته شود.
- ترومبکتومی باز (Open Thrombectomy)
- مشورت با جراح قلب و توراکس در صورت در نظر گرفتن این گزینه.
- در نظر گرفتن ECMO
- نیتریک اکساید (Nitric Oxide) – Inhaled
- کاهش مقاومت عروق ریوی ناشی از وازوکانستریکشن ثانویه به لخته.
- مطالعه iNOPE
- مطالعهای کوچک که نشان میدهد بیماران با تحت فشار قرار گرفتن حاد بطن راست(acute right heart strain) ناشی از PE احتمال بیشتری برای بهبود اتساع یا هایپوکنزی قلب راست در ۲۴ ساعت دارند.
- احیای با مایعات (Fluid resuscitation)
- رویکرد به آمبولی ریوی نیمه گسترده (Submassive PE) با right heart strain
- تعریف: بیمار با فشار خون طبیعی ولی با یافتههای تصویربرداری و بیومارکرهای نشاندهنده استرین قلب راست.
- یافتههای بیومارکری نشاندهنده استرین قلب راست:
- BNP >90 pg/mL یا pro BNP >900 pg/mL
- تروپونین – افزایش حاد مشکوک بالاتر از محدوده مرزی گزارششده آزمایشگاه یا بیشتر.
- یافتههای بیومارکری نشاندهنده استرین قلب راست:
- درمان در این موارد مورد اختلاف(controversial) است
- برخی بیماران ممکن است از ترومبولیز سود ببرند، اما هنوز مشخص نیست چه کسی کاندیدای مناسب است و دوز مناسب آلتپلاز چه مقدار است.
- ارزیابی فایده/ضرر، میزان شوک/هایپوکسی، و مشورت با متخصصان ضروری است.
- ضد انعقاد
- تعریف: بیمار با فشار خون طبیعی ولی با یافتههای تصویربرداری و بیومارکرهای نشاندهنده استرین قلب راست.
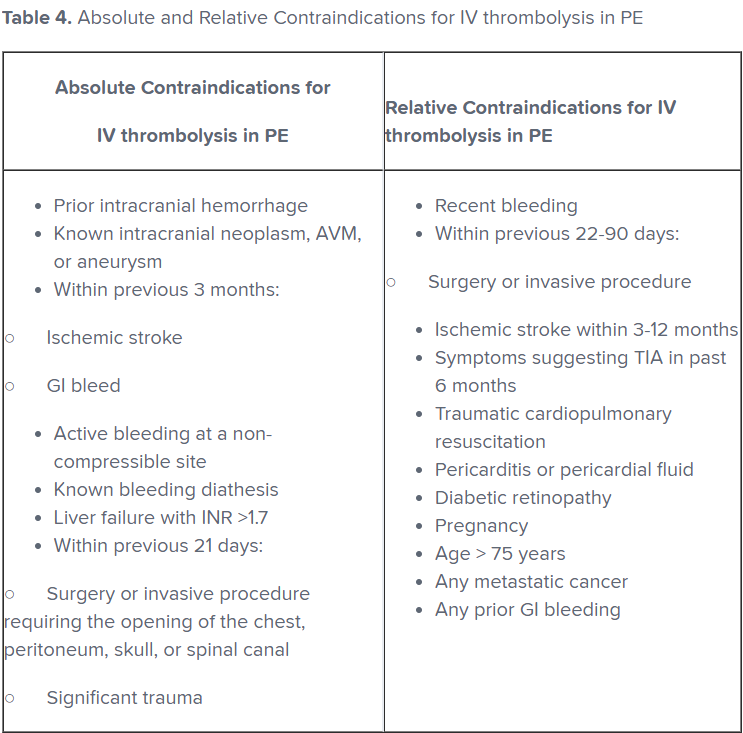
*اقتباس شده از Garrett J (2019)
منبع:
https://www.emrap.org/c3/playlist/cardiovascular/episode/c3pulmonary/c3pulmonary